一、往複筒法的來源
口服藥物(wù)的生物(wù)利用(yòng)度與治療效果主要取決于制劑在胃腸道中(zhōng)的釋放與吸收。快吸收的藥物(wù),溶出快慢是藥物(wù)吸收的限速步驟。因此對于口服固體(tǐ)制劑的開發、質(zhì)量控制、上市後的監管來說,溶出度是一項重要的檢測指标。
USP1法是1970年被美國(guó)藥典首先采用(yòng)的,USP2法在1978年被認可(kě),但是這兩種方法并不能(néng)連續的改變介質(zhì)pH。随着緩控釋制劑的出現,為(wèi)了獲得體(tǐ)外溶出與生物(wù)利用(yòng)度之間的相關性(體(tǐ)外-體(tǐ)内相關性),藥物(wù)溶出度測試需要使用(yòng)不同pH的介質(zhì)、離子強度、粘度和攪拌速度等,從而更好的模拟制劑通過胃腸道的過程。為(wèi)了解決這個問題,倫敦大學(xué)研究人員以A.H.Beckett 為(wèi)首,基于片劑崩解裝(zhuāng)置設計了往複筒法,此方法能(néng)夠實現連續更換不同pH介質(zhì),并作(zuò)為(wèi)USP3 法于1991年收入了《美國(guó)藥典》,逐漸用(yòng)于緩控釋制劑的溶出方法開發。
二、往複筒法介紹
往複筒法主要由防蒸發帽、内管、玻璃溶出杯、水浴箱等組成。
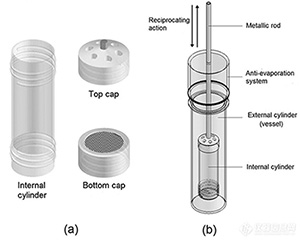
試驗時把藥物(wù)放在玻璃内管中(zhōng),玻璃内管與往複筒軸相連接,往複筒軸上下往複運動時水流不停的沖擊内管的藥物(wù)。當第一排運行結束後,往複筒軸自動移動到下一行,再次浸沒藥物(wù)并且繼續往複動作(zuò)。
往複筒法的溶出杯與傳統的籃、槳法的溶出杯有(yǒu)較大的差異,溶出杯底部是平底設計而且容量僅為(wèi)300mL。在溶出杯上端有(yǒu)防蒸發系統,避免溶出介質(zhì)體(tǐ)積的顯著變化。此外為(wèi)了滿足實驗條件,往複筒可(kě)以使用(yòng)不同體(tǐ)積的溶出杯,如碳酸镧咀嚼片的溶出則使用(yòng)1000mL的溶出杯。
三、往複筒法的應用(yòng)
3.1緩控釋與腸溶性制劑
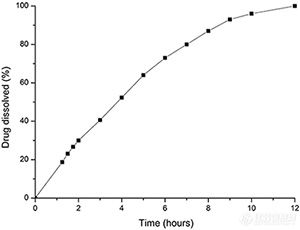
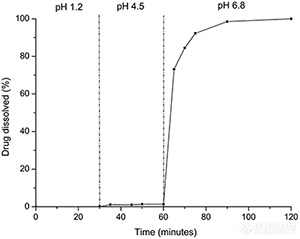
改良釋放劑型較傳統制劑有(yǒu)很(hěn)大的優勢,但在體(tǐ)内經曆的環境更為(wèi)複雜。因此在體(tǐ)外能(néng)夠模拟出與體(tǐ)内相似的環境,有(yǒu)利于其質(zhì)量特性的評價。往複筒法能(néng)夠模拟出體(tǐ)内環境,可(kě)以使藥物(wù)經曆不同的pH值的環境,如圖所示:
|
|
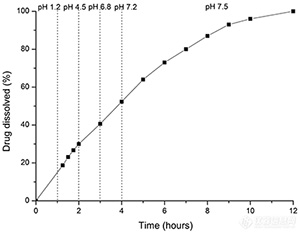
相比于傳統的溶出方法,往複筒法可(kě)以獲得藥物(wù)在不同pH下的溶出數據 | |
|
|
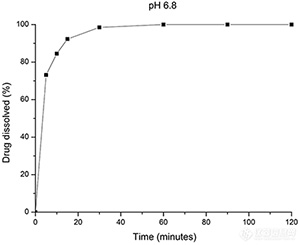
對于腸溶性制劑,往複筒法可(kě)做耐酸性試驗 | |
3.2速釋制劑
雖然往複筒法設計初衷為(wèi)了解決緩控釋制劑釋放度問題,随着對往複筒法深入研究,發現其能(néng)夠适用(yòng)部分(fēn)口服速釋制劑。如在常規溶出試驗中(zhōng),發現制劑粘附在溶出杯上、漂浮在介質(zhì)表面、輔料堵住籃孔、藥物(wù)粉末堆積等異常的物(wù)理(lǐ)現象,往複筒法憑借其獨特的運動方式可(kě)以避免以上問題。對于咀嚼片使用(yòng)玻璃珠可(kě)以模拟咀嚼力從而獲得與體(tǐ)内相關的釋放行為(wèi)。軟膠囊因為(wèi)囊殼的差異,其溶出重現性較差,在往複筒中(zhōng)添加惰性物(wù)質(zhì)有(yǒu)利于RSD的降低。為(wèi)了提高溶出液中(zhōng)主成份的檢測靈敏度,往複筒法同樣适用(yòng)小(xiǎo)規格制劑的溶出。
四、結語
在評估制劑的體(tǐ)外溶出特性方面,往複筒法與籃槳法相比具(jù)有(yǒu)很(hěn)大的優勢。不僅限于緩釋産(chǎn)品,還可(kě)以用(yòng)于其他(tā)固體(tǐ)口服劑型,例如速釋片劑、咀嚼片、軟膠囊等。同時它可(kě)以模拟體(tǐ)内環境,如進食和禁食狀态更好的獲取與體(tǐ)内相關的釋放行為(wèi)。
參考文(wén)獻:Applicationsof USP apparatus 3 in assessing the in vitro release of solid oraldosage forms,BrazilianJournal of Pharmaceutical Sciences vol.51,n.2,apr./jun.2015




 客服1
客服1